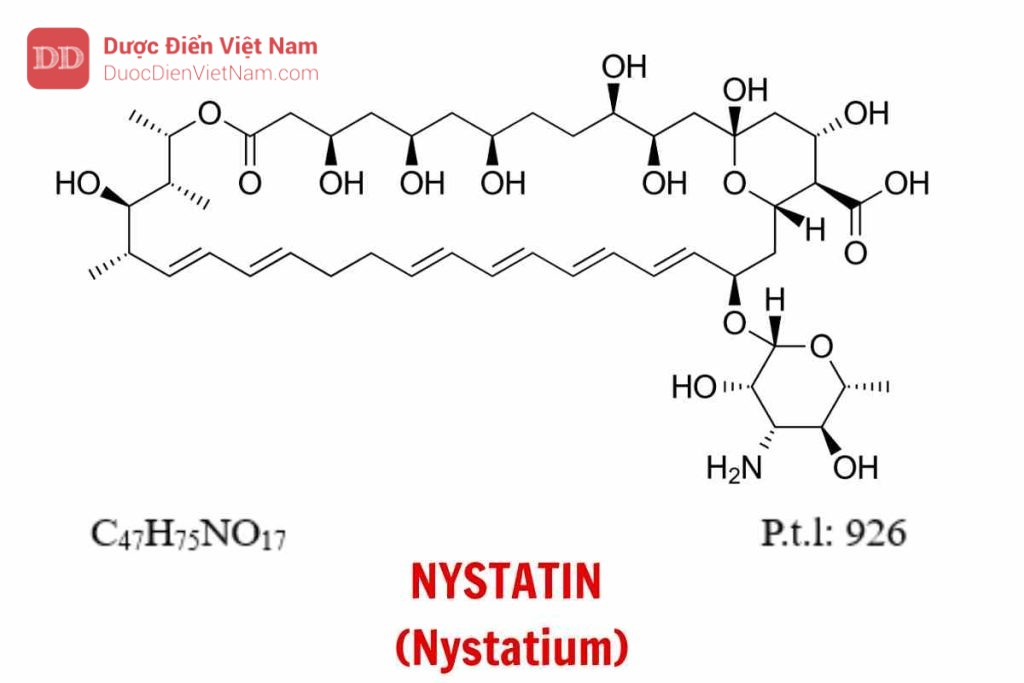
NYSTATIN (Nystatium) – Dược điển Việt Nam 5
Nếu nội dung bài viết chưa chính xác, vui lòng thông báo cho chúng tôi tại đâyNystatin là một chất chống nấm, được sản xuất bằng cách lên men sử dụng một số chủng Streptomyces noursei, chứa chủ yếu là các tetraen, thành phần chính là acid (1S, 3R,4R,7R,9R,11R, 15S,16R,17R,18S,19E,21E,25E,27E,29E,31E,33E,35S,36E,37S)-33-[(3-amino-3,6-dideoxy-β-D-mannopyranosyl)oxy]-1,3,4,7,9,11,17,37-octahydroxy 15,16,18-trimethyl-13-oxo-14,39-dioxabicyclo [33.3.1]nonatriaconta-19,21,25,27,29,31 -hexaen-36-carboxylic(nystatin A1). Hoạt lực không được dưới 4400 IU/mg và không được dưới 5000 IU/mg nếu dùng để sản xuất thuốc dùng đường uống, tính theo chế phẩm đã làm khô.
Sản xuất
Nếu chế phẩm không dùng để sản xuất thuốc ngoài da, phương pháp sản xuất phải được đánh giá để chứng tỏ rằng chế phẩm nếu được thử phải đạt yêu cầu của phép thử sau:
Độc tính bất thường (Phụ lục 13.5)
Tiêm trong màng bụng mỗi chuột nhắt 0,5 ml hỗn dịch chế phẩm trong dung dịch acacia 0,5 % có chứa không dưới 600 IU.
Tính chất
Bột màu vàng hoặc nâu nhạt, dễ hút ẩm.
Thực tế không tan trong nước và trong ethanol 96 %, dễ tan trong dimethylfomamid và dimethyl sulfoxid, khó tan trong methanol.
Định tính
Có thể chọn một trong hai nhóm định tính sau:
Nhóm I: A, E.
Nhóm II: B, C, D.
A. Phổ hấp thụ hồng ngoại (Phụ lục 4.2) của chế phẩm phải phù hợp với phổ hồng ngoại của nystatin đối chiếu.
B. Phổ hấp thụ tử ngoại (Phụ lục 4.1) của dung dịch ở phép thử Độ hấp thụ ánh sáng, có 4 cực đại hấp thụ ở 230; 291; 305 và 319 nm và một vai ở 280 nm. Tỷ lệ độ hấp thụ giữa các cực đại 291 nm và 319 nm so với độ hấp thụ cực đại ở 305 nm lần lượt từ 0,61 đến 0,73 và từ 0,83 đến 0,96.
Tỷ lệ giữa độ hấp thụ cực đại ở 230 nm so với độ hấp thụ ở 280 nm từ 0,83 đến 1,25.
C. Thêm 0,1 ml acid hydrocloric (TT) vào khoảng 2 mg chế phẩm. Xuất hiện màu nâu.
D. Thêm 0,1 ml acid sulfuric (TT) vào khoảng 2 mg chế phẩm. Xuất hiện màu nâu, màu chuyển thành tím khi để lâu.
E. Trong phần Thành phần nystatin, pic chính trên sắc ký đồ của dung dịch thử phải tương ứng với pic chính trên sắc ký đồ của dung dịch đối chiếu (1)
Độ hấp thụ ánh sáng
Hòa tan 0,10 g chế phẩm trong một hỗn hợp gồm 5,0 ml acid acetic băng (TT) và 50 ml methanol (TT), thêm methanol (TT) vừa đủ 100,0 ml. Pha loãng 1,0 ml dung dịch thu được thành 100,0 ml với methanol (TT). Độ hấp thụ (Phụ lục 4.1) của dung dịch thu được ở cực đại hấp thụ 305 nm không được nhỏ hơn 0,60, đo trong vòng 30 min sau khi pha.
Thành phần nystatin
Phương pháp sắc ký lỏng (Phụ lục 5.3), áp dụng phương pháp chuẩn hóa để tính kết quả, tiến hành trong điều kiện tránh ánh sáng.
Pha động A: Acetonitril – dung dịch amoni acetat 0,385 % (29:71)
Pha động B: Acetonitril – dung dịch amoni acetat 0,385 % (60:40)
Dung dịch thử: Hòa tan 20 mg chế phẩm trong dimethyl sulfoxid (TT) và pha loãng thành 50 ml với cùng dung môi.
Dung dịch đối chiếu (1): Hòa tan 20 mg nystatin chuẩn trong dimethyl Sulfoxid (TT) và pha loãng thành 50 ml với cùng dung môi.
Dung dịch đối chiếu (2): Hòa tan 20 mg chế phẩm trong 25 ml methanol (TT) và pha loãng thành 50 ml với nước. Thêm 2,0 ml dung dịch acid hydrocloric loãng (TT) vào 10,0 ml dung dịch thu được, để yên trong 1 h.
Dung dịch đối chiếu (3): Pha loãng 1,0 ml dung dịch đối chiếu (1) thành 100,0 ml bằng dimethyl sulfoxid (TT). Pha loãng 1,0 ml dung dịch thu được thành 10,0 ml với dimethyl sulfoxid (TT).
Điều kiện sắc ký:
Cột kích thước ( 15 cm X 4,6 mm) được nhồi pha tĩnh base- deactivaled end-capped octadecvisilyl silica gel dùng cho sắc ký (5 μm).
Nhiệt độ cột: 30 °C.
Detector quang phổ tử ngoại đặt ở bước sóng 305 nm.
Tốc độ dòng: 1,0 ml/min.
Thể tích tiêm: 20 μl.
Cách tiến hành:
Tiến hành sắc ký với chương trình dung môi như sau:
| Thời gian (min) | Pha động A (%tt/tt) | Pha động B (%tt/tt) |
| 0-25 | 100 | 0 |
| 25-35 | 100-0 | 0-100 |
| 35-45 | 0 | 100 |
| 45-50 | 0-100 | 100-0 |
| 50-55 | 100 | 0 |
Kiểm tra tính phù hợp của hệ thống: Tiến hành sắc ký với dung dịch đối chiếu (2), độ phân giải giữa 2 pic chính (thời gian lưu khoảng 13 min và 19 min) ít nhất là 3,5.
Tiến hành sắc ký với dung dịch thử, dung dịch đối chiếu (1) và dung dịch đối chiếu (3).
Trên sắc ký đồ của dung dịch thử, diện tích của pic nystatin (thời gian lưu khoảng 14 min) không được dưới 85,0 % tổng diện tích các pic, diện tích của bất kỳ pic nào khác không được lớn hơn 4,0 % tổng diện tích các pic. Bỏ qua các pic có diện tích nhỏ hơn diện tích pic chính trên sắc ký đồ của dung dịch đối chiếu (3) và các pic có thời gian lưu nhỏ hơn 2 min.
Kim loại nặng
Không được quá 20 phần triệu (Phụ lục 9-4.8).
Lấy 1,0 g chế phẩm tiến hành theo phương pháp 3. Dùng 2 ml dung dịch chì mẫu 10 phần triệu Pb (TT) để chuẩn bị mẫu đối chiếu.
Mất khối lượng do làm khô
Không được quá 5,0 % (Phụ lục 9.6).
(1,000 g; phosphor pentoxyd, 60 °C; áp suất không quá 0,1 kPa; 3 h).
Tro sulfat
Không được quá 3,5 % (Phụ lục 9.9, phương pháp 2).
Dùng 1,0 g chế phẩm.
Định lượng
Tiến hành theo Phụ lục 13.9 Xác định hoạt lực kháng sinh bằng phương pháp thử vi sinh vật. Chú ý tránh ánh sáng trong quá trình định lượng.
Dung dịch chuẩn: Cân chính xác khoảng 75 mg nystatin chuẩn vào bình định mức 50 ml, hòa tan trong dimethylformamid (TT) và thêm vừa đủ đến vạch với cùng dung môi. Pha loãng dung dịch thu được bằng dung dịch đệm số 19 để thu được các dung dịch làm việc.
Dung dịch thử: Tiến hành tương tự dung dịch chuẩn.
Bảo quản
Trong bao bì kín, tránh ánh sáng. Nhãn phải ghi rõ nếu chế phẩm chỉ dùng để pha chế thuốc dùng ngoài da.
Loại thuốc
Thuốc chống nấm.
Chế phẩm
Viên nén, thuốc đặt âm đạo, kem, mỡ dùng ngoài.