ĐỊNH LƯỢNG NITROGEN TRONG HỢP CHẤT HỮU CƠ (Phụ lục 10.9) – Dược điển Việt Nam 5
Nếu nội dung bài viết chưa chính xác, vui lòng thông báo cho chúng tôi tại đâyNitrogen trong hợp chất hữu cơ được định lượng dưới dạng amoniac trong amoni sulfat thu được khi vô cơ hóa các hợp chất hữu cơ có chứa nitrogen với acid sulfuric.
Áp dụng phương pháp I nếu không có chỉ dẫn khác.
Phương pháp I
Dụng cụ
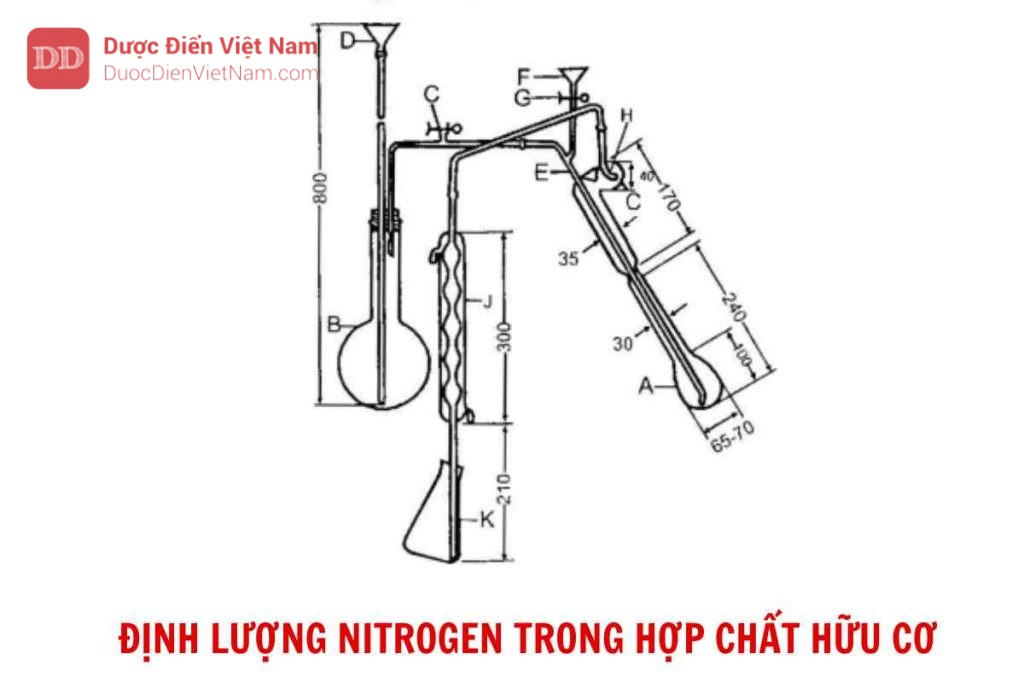
Bộ dụng cụ định lượng nitrogen có thể được chế tạo nguyên bộ chuyên dùng cất amoniac hoặc được lắp ghép từ các dụng cụ thủy tinh cần thiết với nhau sao cho đảm bảo đủ các bộ phận và yêu cầu như Hình 10.9. Các phần bằng cao su của thiết bị nên được xử lý bằng cách đun sôi 10 min đến 30 min trong dung dịch natri hydroxyd 1 M (TT), tiếp theo 30 min đến 60 min trong nước, cuối cùng rửa lại bằng nước trước khi dùng.
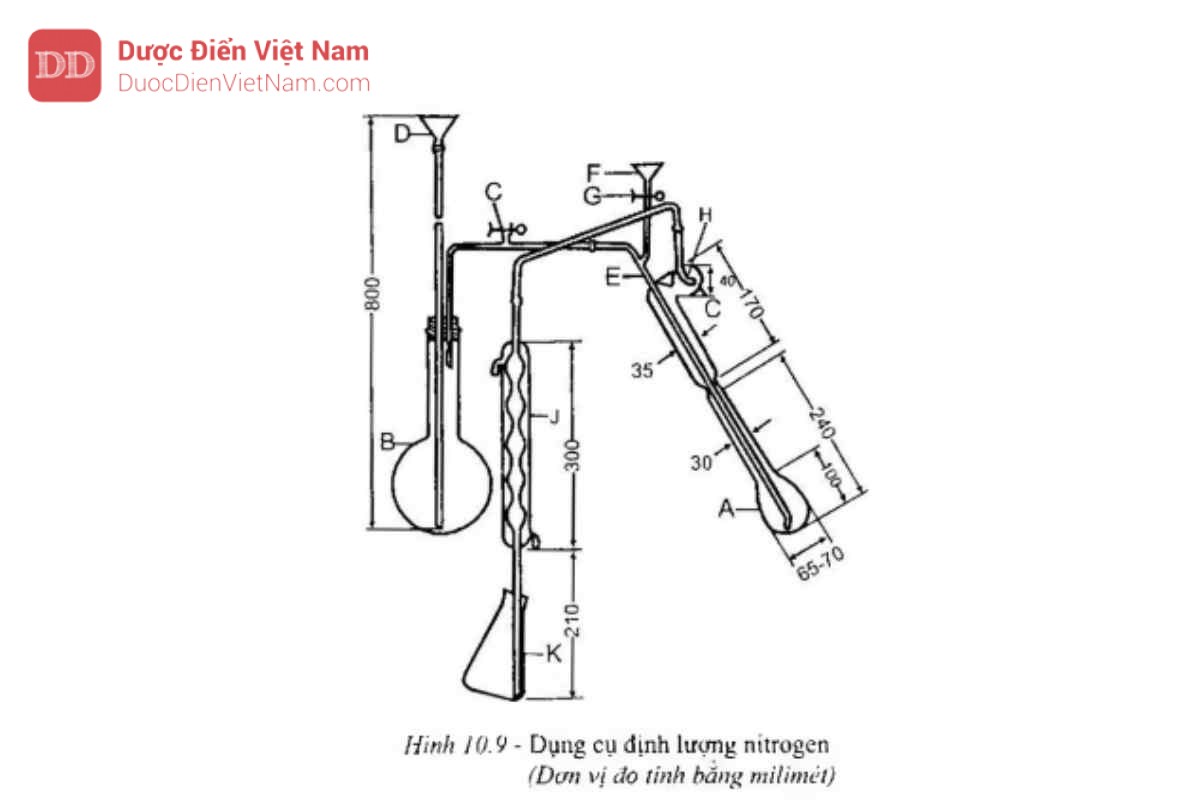
B. Bình cầu để cung cấp hơi nước,
C. Khoá an toàn.
D. Phễu cấp nước vào bình B.
E. Ống dẫn hơi nước từ bình B sang bình phản ứng A.
F. Phễu cấp dung dịch kiềm vào bình phản ứng A.
G. Ống nối bằng cao su có kẹp khóa.
H. Lỗ nhỏ có đường kính bằng đường kính ống cấp hơi.
J. Ống sinh hàn.
K. Bình hứng dịch cất được.
Cách tiến hành
Nếu chuyên luận riêng không có chỉ dẫn gì đặc biệt thì tiến hành như sau:
a. Vô cơ hóa
Lấy chính xác một lượng mẫu thử có chứa khoảng 5 mg nitrogen cho vào bình Kjeldahl A, thêm 1 g hỗn hợp kali sulfat (TT) hoặc natri sulfat khan (TT) và đồng sulfat (TT) (tỷ lệ 10 : 1) đã được tán nhỏ, 7 ml acid sulfuric đậm đặc (TT) và vài viên bi thủy tinh. Đậy bình bằng một phễu có cuống dài. Đặt bình nghiêng 45° trên ngọn lửa nhỏ để hỗn hợp nóng lên từ từ rồi tăng dần nhiệt độ tới khi sôi và tiếp tục đun tới khi chất lỏng trong bình có màu lục tươi và không còn những đốm đen của chất hóa than trên thành bình. Nếu chất lỏng trong bình chưa chuyển sang màu lục tươi, có thể thêm 1 ml đến 2 ml dung dịch hydrogen peroxyd 100 tt (TT) khi đã để nguội và đun tiếp đến khi thu được màu này. Đun thêm 30 min nữa, để nguội.
b. Chuẩn bị cất
Thêm 20 ml nước cất vào bình Kjeldahl đã vô cơ hóa, để nguội trở lại rồi lắp bình này vào bộ dụng cụ cất đã được làm sạch trước bằng cách cho hơi nước chạy qua. Nếu bộ dụng cụ cất amoniac có bình phản ứng A gắn liền thì dùng 20 ml nước cất để chuyên hỗn hợp từ bình Kjeldahl vào bình phản ứng.
Cho nước cất vào khoảng 2/3 bình cấp hơi nước B, thêm vài giọt acid sulfuric (TT) để acid hóa chống sự thâm nhập của amoniac từ không khí. Lấy chính xác 30,0 ml dung dịch acid sulfuric 0,02 N (CĐ) và 2 giọt dung dịch hỗn hợp đỏ methyl (TT) cho vào bình hứng K.
Lắp nối các bộ phận với nhau như hình vẽ sao cho tạo thành một hệ thống kín, đầu cuối của ống sinh hàn thu dịch cất được phải ngập sâu trong dung dịch của bình hứng K.
c. Tiến hành cất
Khi việc chuẩn bị cất đã hoàn tất, cho nước lạnh chảy qua ống sinh hàn và bắt đầu đun nước trong bình B. Khi nước sôi thì cho vào bình phản ứng A qua phễu F từng ít một 30 ml dung dịch natri hydroxyd 40 % (TT) bằng cách sau: đổ hết lượng kiềm này vào phễu F và dùng kẹp G điều chỉnh cho dung dịch kiềm chảy xuống từ từ, khi xong khóa chặt kẹp lại. Tiếp tục cất đến khi hứng được khoảng 100 ml dịch cất. Hạ thấp bình hứng và rửa đầu sinh hàn với một ít nước cất.
d. Chuẩn độ
Chuẩn độ acid sulfuric thừa trong bình hứng dịch cất bằng dung dịch natri hydroxyd 0,02 N (CĐ) tới khi chuyển sang màu vàng, ghi số ml dung dịch natri hydroxyd 0,02 N (CĐ) đã dùng (a ml).
Tiến hành song song một mẫu trắng theo trình tự trên. Ghi số ml dung dịch natri hydroxyd 0,02 N (CĐ) đã dùng (b ml).
Tính kết quả: Lượng nitrogen trong mẫu thử (X) tính bằng gam theo công thức:
X = (b – a) X 0,00028
Trường hợp mẫu thử có lẫn nitrat và nitrit:
Tiến hành tương tự như trên nhưng giai đoạn vô cơ hóa cần tiến hành loại trừ ảnh hưởng của nitrat và nitrit như sau:
Sau khi cho mẫu thử vào bình Kjeldahl A, thêm 10 ml acid sulfuric (TT) đã hòa tan 0,4 g acid salicylic (TT), lắc đều và để yên 30 min (thỉnh thoảng lắc đều). Thêm 2 g natri thiosulfat (TT). Lắc đều, thêm 200 mg bột đồng sulfat khan (TT) rồi tiến hành vô cơ hóa như trên bắt đầu từ “Đặt bình nghiêng 45°… ”
Phương pháp II
Định lượng protein trong các chế phẩm máu
Đối với các chế phẩm máu khô, chuẩn bị dung dịch chế phẩm như chỉ dẫn trong chuyên luận riêng.
Lấy một thể tích chế phẩm tương ứng với 0,1 g protein, pha loãng thành 20 ml bằng dung dịch natri clorid 0,9 % (TT). Lấy 2 ml dung dịch thu được chuyển vào ống nghiệm dung tích 75 ml, thêm 2 ml dung dịch chứa 75 % acid sulfuric không có nitrogen (TT), 4,5 % kali sulfid (TT) và 0,5 % đồng Sulfat (TT), trộn đều và đậy ống nghiệm một cách lỏng lẻo. Đun nóng từ từ đến sôi và tiếp tục đun sôi mạnh trong khoảng 1,5 h và để nguội. Nếu dung dịch thu được không trong thì thêm 0,25 ml dung dịch dung dịch hydrogen peroxyd 20 tt (TT) và đun tiếp đến khi thu được dung dịch trong và để nguội. Trong quá trình đun, chú ý không để phần trên của ống nghiệm bị nóng quá.
Chuyển dung dịch thu được vào bộ dụng cụ cất, dùng nước tráng rửa 3 lần, mỗi lần 3 ml. Thêm vào bình cất 10 ml dung dịch natri hydroxyd 10 M (TT) và cất nhanh trong vòng 4 min. Hứng dịch cất vào trong hỗn hợp 5 ml dung dịch acid boric bão hòa (TT) và 5 ml nước, giữ đầu cuối của ống sinh hàn ngập trong dịch hứng. Hạ thấp bình hứng để đầu ống sinh hàn không còn ngập trong dịch hứng và tiếp tục cất thêm 1 min nữa. Chuẩn độ bằng dung dịch acid hydrocloric 0,02 N (CĐ) dùng dung dịch hỗn hợp đỏ methyl (TT) làm chỉ thị (V1).
Lấy một thể tích chế phẩm tương ứng với 0,1 g protein, thêm 12 ml dung dịch natri clorid 0,9 % (TT), thêm 2 ml dung dịch natri molybdat 7,5 % và 2 ml hỗn hợp acid sulfuric không có nitrogen – nước (1 : 30). Lắc đều, để yên 15 min và thêm nước vừa đủ 20 ml. Lắc và ly tâm. Lấy 2 ml dịch ly tâm ở trên chuyển vào ống nghiệm dung tích 75 ml và tiếp tục tiến hành như trên, bắt đầu từ: “thêm 2 ml dung dịch chứa 75 % acid sulfuric không có nitrogen…” (V2). Tính hàm lượng protein trong chế phẩm X (mg/ml) áp dụng công thức sau (cần tính đến hệ số pha loãng ban đầu):
X = 6,25 X 0,280(V1 – V2)