HEPTAMINOL HYDROCLORID (Heptaminoli hydrochloridum) – Dược Điển Việt Nam 5
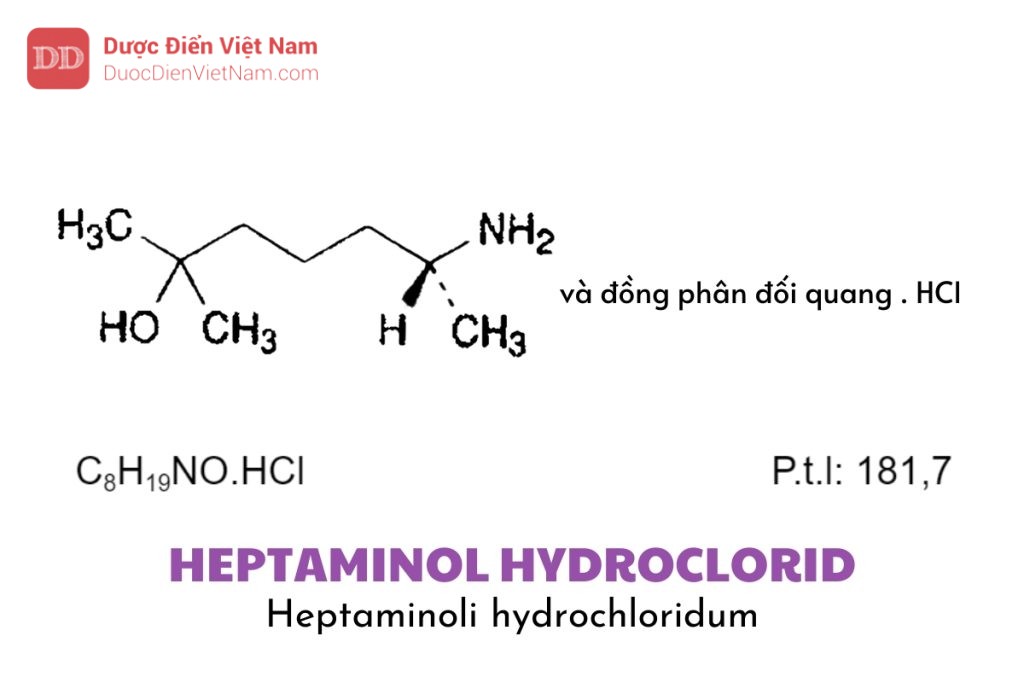
Nếu nội dung bài viết chưa chính xác, vui lòng thông báo cho chúng tôi tại đâyHeptaminol hydroclorid là (6RS)-6-amino-2-methyl-heptan-2-ol hydroclorid, phải chứa từ 99,0 % đến 101,0 % C8H19NO.HCl, tính theo chế phẩm đã làm khô.
Tính chất
Bột kết tinh trắng hay gần như trắng.
Dễ tan trong nước, tan trong ethanol 96 %, thực tế không tan trong methylen clorid.
Định tính
Có thể chọn một trong hai nhóm định tính sau:
Nhóm I: A, D.
Nhóm II: B, C, D.
A. Phổ hấp thụ hồng ngoại (Phụ lục 4.2) của chế phẩm phải phù hợp với phổ hấp thụ hồng ngoại của heptaminol hydroclorid chuẩn.
B. Ở mục Tạp chất liên quan, quan sát dưới ánh sáng ban ngày, dung dịch thử (2) phải cho vết chính có vị trí, màu sắc và kích thước tương ứng với vết chính của dung dịch đối chiếu (2).
C. Thêm 4 ml nước và 2 ml dung dịch amoni ceri nitrat 20 % trong dung dịch acid nitric 4 M vào 1 ml dung dịch S, màu nâu da cam xuất hiện.
D. Chế phẩm phải cho phản ứng (A) của clorid (Phụ lục 8.1).
=> Đọc thêm: VIÊN NÉN HALOPERIDOL (Tabellae Haloperidoli) – Dược Điển Việt Nam 5.
Độ trong và màu sắc của dung dịch
Dung dịch S: Hòa tan 5,0 g chế phẩm trong nước không có carbon dioxyd (TT) và pha loãng thành 50 ml với cùng dung môi.
Dung dịch S phải trong (Phụ lục 9.2) và có màu không được đậm hơn màu mẫu VN6 (Phụ lục 9.3, phương pháp 2).
Giới hạn acid – kiềm
Thêm 0,1 ml dung dịch đỏ methyl (TT) và 0,3 ml dung dịch acid hydroclorid 0,01 N (CĐ) vào 10 ml dung dịch S, dung dịch phải có màu đỏ. Thêm 0,6 ml dung dịch natri hydroxyd 0,01 N (CĐ) dung dịch phải có màu vàng.
Tạp chất liên quan
Phương pháp sắc ký lớp mỏng (Phụ lục 5.4).
Bản mỏng: Silica gel G.
Dung môi khai triển: Amoniac – dioxan – 2-propanol (10 : 50 : 50).
Dung dịch thử (1): Hòa tan 0,50 g chế phẩm trong methanol (TT) và pha loãng thành 5,0 ml với cùng dung môi.
Dung dịch thử (2): Pha loãng 1,0 ml dung dịch thử (1) thành 10 ml với methanol (TT).
Dung dịch đối chiếu (1): Pha loãng 3,0 ml dung dịch thử (1) thành 10,0 ml với methanol (TT). Pha loãng 1,0 ml dung dịch thu được thành 50,0 ml với methanol (TT).
Dung dịch đối chiếu (2): Hòa tan 0,10 g heptaminol hydroclorid chuẩn trong methanol (TT) và pha loãng thành 10 ml với cùng dung môi.
Dung dịch đối chiếu (3): Hòa tan 10,0 mg tạp chất A chuẩn của heptaminol [(2RS)-6-methylhept-5-en-2-amin)] trong methanol (TT) và pha loãng thành 5,0 ml với cùng dung môi.
Dung dịch đối chiếu (4): Pha loãng 1,0 ml dung dịch đối chiếu (3) thành 10,0 ml với methanol (TT).
Dung dịch đối chiếu (5): Lấy 2,5 ml dung dịch đối chiếu (3), thêm 0,5 ml dung dịch thử (2) và pha loãng thành 5 ml với methanol (TT).
Cách tiến hành: Chấm riêng biệt lên bản mỏng 10 μl dung dịch thử (1), thử (2), đối chiếu (1), (2), (4) và (5). Triển khai sắc ký đến khi dung môi đi được 15 cm. Lấy bản mỏng ra và để khô ngoài không khí. Đặt bản mỏng trong bình bão hòa hơi iod ít nhất 15 h.
Phép thử chỉ có giá trị khi trên sắc ký đồ của dung dịch đối chiếu (5) cho 2 vết chính tách nhau rõ ràng và dung dịch đối chiếu (1) cho 1 vết chính.
Trên sắc ký đồ của dung dịch thử (1): vết tương ứng vết tạp chất A không được có màu đậm hơn màu của vết trên sắc ký đồ của dung dịch đối chiếu (4) (0,2 %); bất kỳ vết phụ nào ngoài vết chính và vết tạp chất A không được có màu đậm hơn màu của vết trên sắc ký đồ của dung dịch đối chiếu (1) (0,6 %).
Kim loại nặng
Không được quá 10 phần triệu (Phụ lục 9.4.8).
Lấy 12 ml dung dịch S thử theo phương pháp 1. Dùng dung dịch chì mẫu 1 phần triệu Pb (TT) để chuẩn bị đối chiếu.
Mất khối lượng do làm khô
Không được quá 0,5 % (Phụ lục 9.6).
(1,000 g; 105 °C;4h).
Tro sulfat
Không được quá 0,1 % (Phụ lục 9.9, phương pháp 2).
Dùng 1,0 g chế phẩm.
Định lượng
Hòa tan 0,140 g chế phẩm trong 50 ml ethanol 96 % (TT) và thêm 5,0 ml dung dịch acid hydrocloric 0,01 N (CĐ). Chuẩn độ bằng dung dịch natri hydroxyd 0,1 N (CĐ). Xác định điểm kết thúc bằng phương pháp chuẩn độ đo điện thế (Phụ lục 10.2). Đọc thể tích đã tiêu thụ giữa 2 điểm uốn.
1 ml dung dịch natri hydroxyd 0,1 N (CĐ) tương ứng với 18,17 mg C8H19NO.HCl.
=> Đọc thêm: HALOTHAN (Halothanum) – Dược Điển Việt Nam 5.
Bảo quản
Trong đồ đựng kín.
Loại thuốc
Thuốc điều trị hạ huyết áp.
Chế phẩm
Viên nén.