HYDROXOCOBALAMIN CLORID (Hydroxocobalamini chloridum) – Dược Điển Việt Nam 5
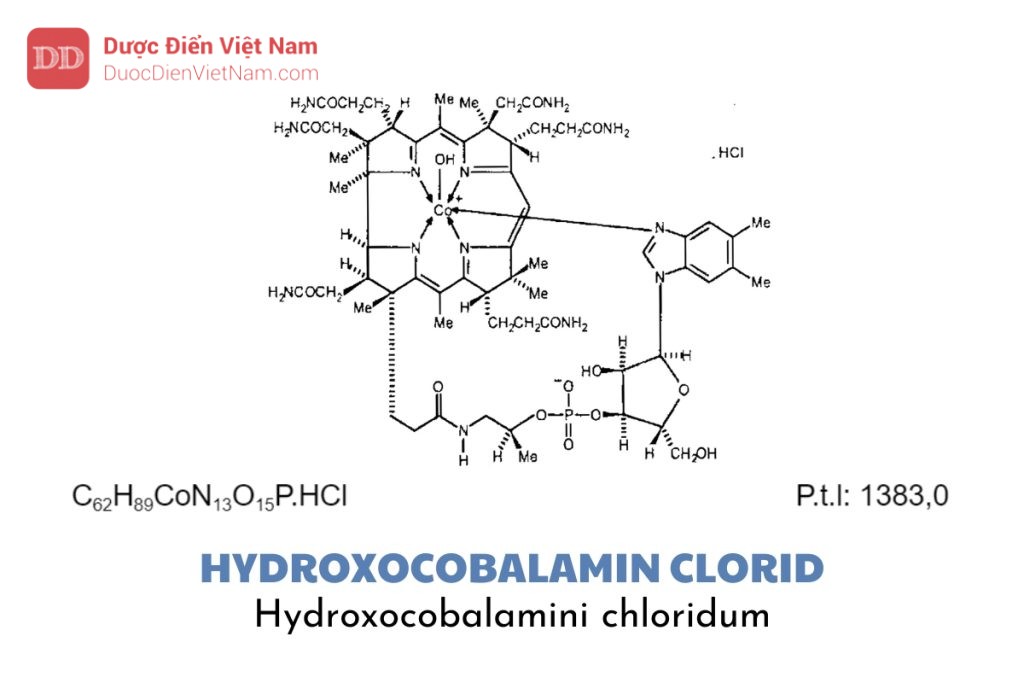
Nếu nội dung bài viết chưa chính xác, vui lòng thông báo cho chúng tôi tại đâyHydroxocobalamin clorid là Coα-[α-(5,6-dimethyl benzimidazolyl)]-Coβ-hydroxocobalamid clorid, phải chứa từ 96,0 % đến 102,0 % C62H89CoN13O15P. HCl, tính theo chế phẩm đã làm khô.
Tính chất
Bột kết tinh hoặc tinh thể màu đỏ đậm, tan trong nước và rất hút ẩm. Có thể bị phân hủy khi sấy khô.
Định tính
A. Hòa tan 2,5 mg chế phẩm trong dung dịch có chứa 0,8 % (tt/tt) acid acetic khan (TT) và 1,09 % natri acetat (TT) rồi pha loãng thành 100 ml với cùng dung môi. Phổ hấp thụ tử ngoại – khả kiến (Phụ lục 4.1) của dung dịch trên trong khoảng bước sóng 260 nm đến 610 nm có ba đỉnh hấp thụ cực đại ở bước sóng 274 nm, 351 nm và 525 nm. Tỷ số độ hấp thụ ở bước sóng 274 nm so với độ hấp thụ ở bước sóng 351 nm từ 0,75 đến 0,83. Tỷ số độ hấp thụ ở bước sóng 525 nm so với độ hấp thụ ở bước sóng 351 nm từ 0,31 đến 0,35.
B. Phương pháp sắc ký lớp mỏng (Phụ lục 5.4).
Bản mỏng: Silica gel G.
Dung môi khai triển: Dung dịch amoniac 10 % – methanol (25 : 75).
Dung dịch thử: Hòa tan 2 mg chế phẩm trong 1 ml dung dịch đồng thể tích ethanol 96 % (TT) và nước.
Dung dịch đối chiếu: Hòa tan 2 mg hydroxocobalamin clorid chuẩn trong 1 ml dung dịch đồng thể tích ethanol 96 % (TT) và nước.
Cách tiến hành: Tiến hành tránh ánh sáng.
Chấm riêng biệt lên bản mỏng 10 μl mỗi dung dịch trên.
Triển khai sắc ký trong bình sắc ký không bão hòa dung môi đến khi dung môi đi được 12 cm. Để bản mỏng khô ngoài không khí và quan sát dưới ánh sáng ban ngày, vết chính trong sắc ký đồ của dung dịch thử phải phù hợp với vết chính trong sắc ký đồ của dung dịch đối chiếu về vị trí, màu sắc và kích thước.
C. Chế phẩm phải cho phản ứng của clorid (Phụ lục 8.1).
=> Tham khảo: HYDROXOCOBALAMIN ACETAT (Hydroxocobalamini acetas) – Dược Điển Việt Nam 5.
Tạp chất liên quan
Phương pháp sắc ký lỏng (Phụ lục 5.3), dùng các dung dịch mới pha và tiến hành tránh ánh sáng.
Pha động: 19,5 thể tích methanol (TT) và 80,5 thể tích dung dịch có chứa 1,5 % acid citric (TT) và 0,81 % dinatri hydrophosphat (TT) trong nước.
Dung dịch thử: Hòa tan 10,0 mg chế phẩm trong pha động vừa đủ 10,0 ml.
Dung dịch đối chiếu (1): Pha loãng 5,0 ml dung dịch thử thành 100,0 ml bằng pha động.
Dung dịch đối chiếu (2): Pha loãng 1,0 ml dung dịch thử thành 10,0 ml bằng pha động. Pha loãng 1,0 ml dung dịch thu được thành 100,0 ml bằng pha động.
Dung dịch phân giải: Hòa tan 25 mg chế phẩm trong 10 ml nước, làm nóng nếu cần thiết. Để nguội và thêm 1 ml dung dịch cloramin T 2 % (TT), 0,5 ml dung dịch acid hydrocloric 0,05 M (TT), pha loãng thành 25 ml bằng nước. Lắc, để yên trong 5 min và tiêm ngay.
Điều kiện sắc ký:
Cột kích thước (25 cm x 4 mm) nhồi pha tĩnh B (5 μm).
Detector quang phổ tử ngoại đặt ở bước sóng 351 nm.
Tốc độ dòng: 1,5 ml/min.
Thể tích tiêm: 20 μl.
Cách tiến hành:
Tiến hành sắc ký với thời gian gấp 4 lần thời gian lưu của pic chính trên sắc ký đồ của dung dịch đối chiếu (1).
Phép thử chỉ có giá trị khi trên sắc ký đồ của dung dịch phân giải có 3 pic chính và hệ số phân giải giữa hai pic gần nhau. Ít nhất là 3,0; sắc ký đồ của dung dịch đối chiếu (2) có 1 pic chính và tỷ số tín hiệu của pic này so với độ nhiễu đường nên ít nhất là 5.
Giới hạn: Trong sắc ký đồ của dung dịch thử:
Tổng diện tích của các pic phụ ngoài pic chính không được lớn hơn diện tích pic chính thu được trong sắc ký đồ của dung dịch đối chiếu (1) (5 %).
Bỏ qua tất cả các pic mà diện tích của chúng nhỏ hơn diện tích của pic chính trong sắc ký đồ của dung dịch đối chiếu (2).
Mất khối lượng do làm khô
Từ 8,0 đến 12,0 % (Phụ lục 9.6).
(0,400 g; 100 °C đến 105 °C; áp suất không quá 0,7 kPa).
Định lượng
Cần phải tránh ánh sáng trong quá trình định lượng.
Hòa tan 25,0 mg chế phẩm trong dung dịch có chứa 0,8 % (tt/tt) acid acetic khan (TT) và 1,09 % natri acetat (TT), rồi pha loãng đến 1000,0 ml bằng cùng dung môi. Đo độ hấp thụ (Phụ lục 4.1) của dung dịch trên ở bước sóng cực đại 351 nm. Tính hàm lượng C62H89CoN13O15P. HCl theo A (1 %, 1 cm), lấy 190 là giá trị A(1 %, 1 cm) ở 351 nm.
=> Xem thêm: THUỐC NHỎ MẮT HYDROCORTISON VÀ NEOMYCIN (Collyrium Hydrocortisoni et Neomycini) – Dược Điển Việt Nam 5.
Bảo quản
Trong bao bì kín, ở nhiệt độ từ 2 °C đến 8 °C, tránh ánh sáng.
Loại thuốc
Vitamin B12.