INDINAVIR SULFAT (Indinaviri sulfas) – Dược Điển Việt Nam 5
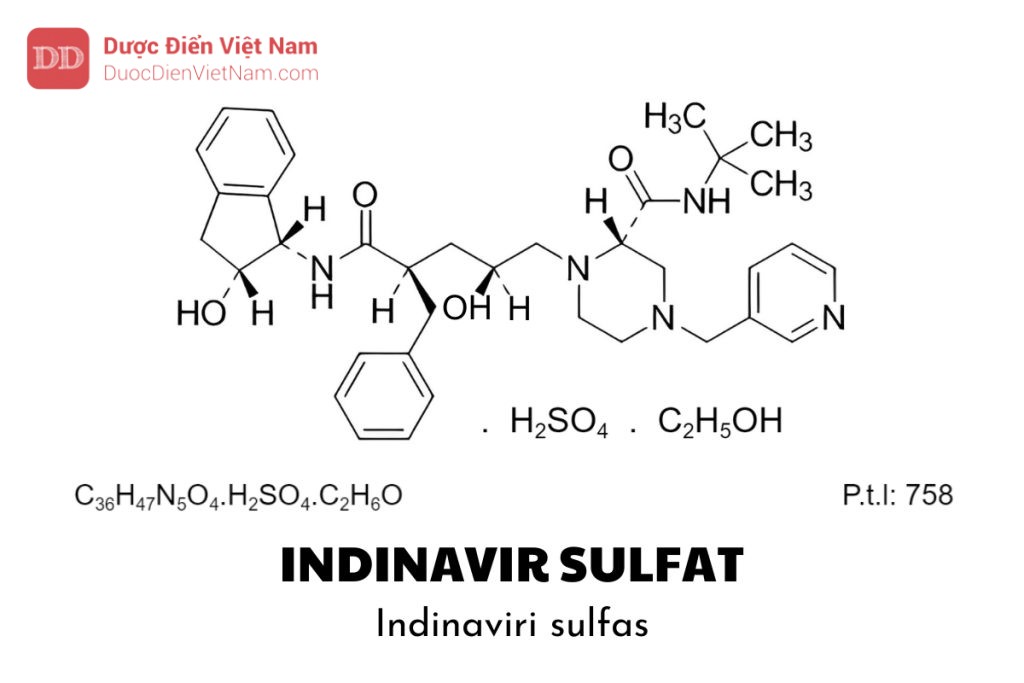
Nếu nội dung bài viết chưa chính xác, vui lòng thông báo cho chúng tôi tại đâyIndinavir sulfat là (2S)-1-[(2S,4R)-4-benzyl-2-hydroxy-5-[[(1S,2R)-2-hydroxy-2,3 -dihydro-1H-inden-1-yl]amino]-5-oxopentyl]-N-(1,1-dimethylethyl)-4-(pyridin-3-ylmethyl)piperazin-2-carboxamid sulfat ethanolat, phải chứa từ 98,0 % đến 102,0 % C36H47N5O4.H2SO4, tính theo chế phẩm khan và không có ethanol.
Trong quá trình sản xuất phải kiểm tra tạp chất đồng phân đối quang trừ phi quy trình sản xuất đảm bảo chọn lọc được đồng phân.
Tính chất
Bột màu trắng hoặc gần như trắng, hút ẩm.
Dễ tan trong nước, tan trong methanol, thực tế không tan trong heptan.
Định tính
A. Phổ hấp thụ hồng ngoại (Phụ lục 4.2) của chế phẩm phải phù hợp với phổ hấp thụ hồng ngoại của indinavir sulfat chuẩn.
B. Góc quay cực riêng (Phụ lục 6.4) của chế phẩm đo ở 25 °C, bước sóng 365 nm phải từ +122° đến +129°, tính theo chất khan và không có ethanol. Hòa tan 0,500 g chế phẩm trong nước và pha loãng thành 50,0 ml với cùng dung môi.
C. Chế phẩm phải cho phản ứng (A) của sulfat (Phụ lục 8.1).
D. Chế phẩm phải đáp ứng phép thử Ethanol.
=> Đọc thêm: INDAPAMID (Indapamidum) – Dược Điển Việt Nam 5.
Tạp chất liên quan
Phương pháp sắc ký lỏng (Phụ lục 5.3).
Pha động A: Dung dịch chứa kali dihỵdrophosphat (TT) nồng độ 0,27 g/l và dikali hydrophosphat (TT) nồng độ 1,40 g/l; lọc và đuổi khí.
Pha động B: Acetonitril (TT1).
Dung dịch A : Hỗn hợp đồng thể tích của pha động A và acetonitril (TT1), trộn đều.
Dung dịch thử: Hòa tan 50,0 mg chế phẩm trong dung dịch A và pha loãng thành 100,0 ml với cùng dung môi.
Dung dịch đối chiếu (1): Hòa tan 4 mg indinavir chuẩn dùng để kiểm tra tính phù hợp của hệ thống sắc ký (chứa tạp chất B, C và E của indinavir) trong dung dịch A và pha loãng thành 10 ml với cùng dung môi.
Dung dịch đối chiếu (2): Pha loãng 1,0 ml dung dịch thử thành 100,0 ml bằng dung dịch A. Pha loãng 1,0 ml dung dịch thu được thành 10,0 ml bằng dung dịch A.
Dung dịch đối chiếu (3): Hòa tan 5,0 mg cis-aminoindanol (tạp chất A) trong dung dịch A và pha loãng thành 10,0 ml với cùng dung môi. Pha loãng 1,0 ml dung dịch thu được thành 100,0 ml bằng dung dịch A. Tiếp tục pha loãng 1,0 ml dung dịch thu được thành 10,0 ml bằng dung dịch A.
Dung dịch đối chiếu (4): Thêm 0,25 ml dung dịch acid hydrocloric 2 M (TT) vào 30 mg chế phẩm và để yên ở nhiệt độ phòng trong vòng 1 h. Thêm hỗn hợp dung môi acetonitril (TT1) – pha động A (2 : 3) vừa đủ 100 ml, lắc đều (thu được hỗn hợp phân hủy có chứa tạp chất D của indinavir).
Điều kiện sắc ký:
Cột kích thước (25 cm x 4,6 mm) được nhồi pha tĩnh C (5 μm).
Detector quang phổ tử ngoại đặt ở bước sóng 220 nm.
Tốc độ dòng: 1,0 ml/min.
Thể tích tiêm: 20 μl.
Cách tiến hành:
Tiến hành sắc ký theo chương trình dung môi sau:
| Thời gian (min) | Pha động A (% tt/tt) | Pha động B (% tt/tt) |
| 0-5 | 80 | 20 |
| 5-40 | 80 → 30 | 20 → 70 |
| 40-45 | 30 | 70 |
| 45-47 | 30 → 80 | 70 → 20 |
| 47-52 | 80 | 20 |
Tiến hành sắc sắc ký với dung dịch đối chiếu (1) và dung dịch đối chiếu (4).
Định tính các tạp chất: Sử dụng sắc ký đồ cung cấp kèm theo indinavir chuẩn dùng để kiểm tra tính phù hợp của hệ thống sắc ký và sắc ký đồ của dung dịch đối chiếu (1) để xác định pic của các tạp chất B, C và E. Sử dụng sắc ký đồ của dung dịch đối chiếu (4) để xác định pic của tạp chất D.
Thời gian lưu tương đối so với indinavir (thời gian lưu khoảng 25 min): Tạp chất A khoảng 0,2; tạp chất B khoảng 0,8; tạp chất C khoảng 0,98; tạp chất D khoảng 1,1; tạp chất E khoảng 1,3.
Kiểm tra tính phù hợp của hệ thống sắc ký: Trên sắc ký đồ của dung dịch đối chiếu (1), độ phân giải giữa pic của tạp chất C và pic của indinavir ít nhất là 1,8.
Tiến hành sắc ký lần lượt với mẫu trắng là dung dịch A, các dung dịch đối chiếu (2), (3) và dung dịch thử.
Giới hạn:
Hệ số hiệu chỉnh: Để tính toán, nhân diện tích pic của tạp chất D với 1,8.
Trên sắc ký đồ thu được từ dung dịch thử:
Diện tích pic tạp chất A không được lớn hơn diện tích pic chính trên sắc ký đồ thu được từ dung dịch đối chiếu (3) (0, 1 %).
Diện tích pic tạp chất D không được lớn hơn 2 lần diện tích pic chính trên sắc ký đồ thu được từ dung dịch đối chiếu (2) (0,2 %).
Diện tích mỗi pic tạp chất B, C, E không được lớn hơn diện tích pic chính trên sắc ký đồ thu được từ dung dịch đối chiếu (2) (0,1 %).
Diện tích mỗi pic tạp chất khác không được lớn hơn 0,5 lần diện tích pic chính trên sắc ký đồ thu được từ dung dịch đối chiếu (2) (0,05 %).
Tổng diện tích của tất cả các pic tạp chất không được lớn hơn 5 lần diện tích pic chính trên sắc ký đồ thu được từ dung dịch đối chiếu (2) (0,5 %).
Bỏ qua các pic tạp chất có diện tích không lớn hơn 0,3 lần diện tích của pic chính trên sắc ký đồ thu được từ dung dịch đối chiếu (2) (0,03 %).
Ghi chú:
Tạp chất A: (1S,2R)-1-amino-2,3-dihydro-1H-inden-2-ol (cis-aminoindanol).
Tạp chất B: (2S)-1-[(2S,4R)-4-benzyl-2-hydroxy-5-[[(1S,2R)- 2-hydroxy-2,3-dihydro-1H-inden-1-yl]amino]-5-oxopentyl]-N- (1,1-dimethylethyl)piperazin-2-carboxamid.
Tạp chất C: (2S)-1-[(2R,4R)-4-benzyl-2-hydroxy-5-[[(1S,2R-2-hydroxy-2,3-dihydro-1H-inden-1-yl]amino]-5-oxopentyl]-N-(1,1-dimethylethyl)-4-(pyridin-3-ylmethyl)piperazin-2-carboxamid.
Tạp chất D: (3R,5S)-3-benzyl-5-[[(2S)-2-[(1,1-dimethylethyl)carbamoyl]-4-(pyridin-3-ylmethyl)piperazin-1-yl]methyl]-4,5-dihydrofuran-2(3H)-on.
Tạp chất E: (2S)-1,4-bis[(2S,4R)-4-benzyl-2-hỵdroxy-5-[[(1S,2R)-2-hydroxy-2,3-dihydro-1H-inden-1-yl]amino]-5-oxopentyl]-N-(1,1-dimethylethy])piperazin-2-carboxamid.
Tạp chất F: 3-(cloromethyl)pyridin (nicotinyl clorid).
Ethanol
Hàm lượng phần trăm của ethanol phải từ 5,0 % đến 8,0 % (kl/kl).
Phương pháp sắc ký khí (Phụ lục 5.2).
Dung dịch chuẩn nội: Pha loãng 1,0 ml propanol (TT) thành 200,0 ml bằng nước.
Dung dịch chuẩn: Pha loãng 1,0 ml ethanol khan (TT) thành 200,0 ml bằng nước. Hút 2,0 ml dung dịch thu được và 2,0 ml dung dịch chuẩn nội, pha loãng thành 25,0 ml bằng nước.
Dung dịch thử: Hòa tan 0,400 g chế phẩm trong 50,0 ml nước, thêm 8,0 ml dung dịch chuẩn nội và pha loãng thành 100,0 ml bằng nước.
Điều kiện sắc ký:
Cột silica nung chảy dài 30 m, đường kính trong 0,53 mm, pha tĩnh là macrogol 20000 (lớp phim dày 1,0 μm).
Khí mang: Heli dùng cho sắc ký khí.
Tốc độ dòng: 10 ml/min.
Tỷ lệ chia dòng: 1 : 10.
Detector ion hóa ngọn lửa.
Nhiệt độ: Duy trì nhiệt độ cột ở 35 °C, nhiệt độ buồng tiêm ở 140 °C và nhiệt độ detector ở 220 °C.
Thể tích tiêm: 1,0 μl.
Cách tiến hành:
Kiểm tra tính phù hợp của hệ thống sắc ký: Trên sắc ký đồ của dung dịch chuẩn, thời gian lưu của ethanol trong khoảng từ 2 min đến 4 min, độ phân giải giữa pic tương ứng với ethanol và propanol ít nhất bằng 5,0.
Tiêm lần lượt dung dịch chuẩn và dung dịch thử. Tính hàm lượng phần trăm (kl/kl) của ethanol trong chế phẩm, tỷ trọng của ethanol là 0,790 g/ml.
=> Xem thêm: VIÊN NÉN INDAPAMID (Tabellae Indapamidi) – Dược Điển Việt Nam 5.
Kim loại nặng
Không được quá 10 phần triệu (Phụ lục 9.4.8).
Hòa tan 2,0 g chế phẩm trong nước và pha loãng thành 20 ml với cùng dung môi. Lấy 12 ml dung dịch thu được tiến hành thử theo phương pháp 1. Dùng dung dịch chì mẫu 1 phần triệu Pb (TT) để chuẩn bị dung dịch đối chiếu.
Nước
Không được quá 1,5 % (Phụ lục 10.3).
Dùng 0,500 g chế phẩm.
Tro sulfat
Không được quá 0,1 % (Phụ lục 9.9, phương pháp 2).
Dùng 1,0 g chế phẩm.
Định lượng
Phương pháp sắc ký lỏng (phụ lục 5.3).
Dung dịch B: Thêm 20 ml dibutylamoni phosphat loại dùng tạo cặp ion vào 1000 ml nước, điều chỉnh về pH 6,5 bằng dung dịch natri hydroxyd 1 M (TT).
Pha động: Acetonitril – dung dịch B (45 : 55).
Dung dịch thử: Hòa tan 60,0 mg chế phẩm trong pha động và pha loãng thành 100,0 ml bằng cùng pha động.
Dung dịch chuẩn: Hòa tan 50,0 mg indinavir chuẩn trong pha động và pha loãng thành 100,0 ml bằng cùng pha động.
Điều kiện sắc ký:
Cột kích thước (25 cm x 4,6 mm) được nhồi base-deactivated octylsilyl silica gel dùng cho sắc ký (5 μm).
Nhiệt độ cột: 40 °C.
Detector quang phổ tử ngoại đặt ở bước sóng 260 nm.
Tốc độ dòng: 1,0 ml/min.
Thể tích tiêm: 10 μl.
Cách tiến hành:
Tiến hành sắc ký các dung dịch chuẩn và dung dịch thử với thời gian gấp hai lần thời gian lưu của pic indinavir (thời gian lưu của pic indinavir khoảng 10 min).
Tính hàm lượng phần trăm indinavir sulfat, C36H47N5O4.H2SO4, trong chế phẩm dựa vào diện tích pic indinavir trên sắc ký đồ thu được từ dung dịch thử, dung dịch chuẩn và hàm lượng C36H47N5O4 trong indinavir chuẩn nhân với hệ số hiệu chỉnh 1,1598.
Bảo quản
Trong đồ đựng kín, tránh ánh sáng.
Loại thuốc
Ức chế enzym protease, kháng HIV.
Chế phẩm
Nang.