PIPERACILIN NATRl (Piperacillinum natricum) – Dược Điển Việt Nam 5
Nếu nội dung bài viết chưa chính xác, vui lòng thông báo cho chúng tôi tại đây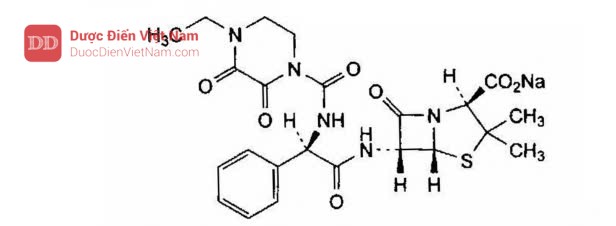
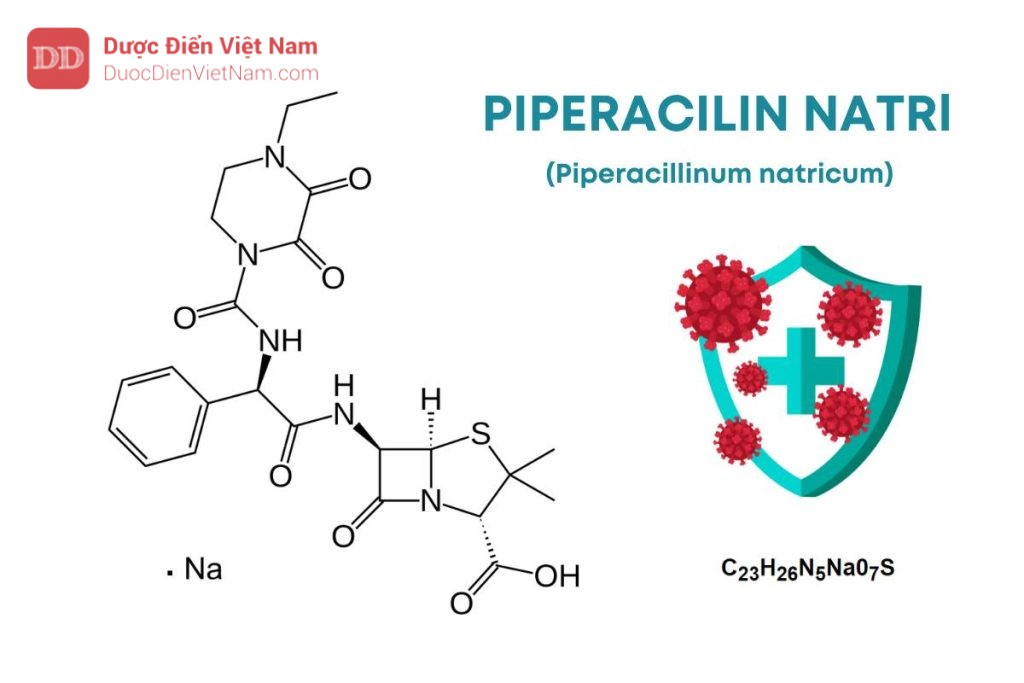
C23H26N5Na07S P.t.l: 539,5
Piperacilin natri là natri (2S,5R,6R)-6-[[(2R)-2-[[(4-ethyl- 2,3-dioxopiperazin-1-yl) carbonyl] amino]-2-phenylacetyl] amino]-3,3-dimethyl-7-oxo-4-thia-1-azabicyclo[3.2.0] heptan-2-carboxylat, phải chứa từ 95,0 % đến 102,0 % C23H26N5Na07S, tính theo chế phẩm khan.
Chế phẩm bán tổng hợp từ một sản phẩm lên men.
Tính chất
Bột màu trắng hay gần như trắng, dễ hút ẩm.
Dễ tan trong nước và methanol, thực tế không tan trong ethyl acetat.
Định tính
A. Hòa tan 0,250 g chế phẩm trong nước, thêm 0,5 ml dung dịch acid hydrocloric loãng (TT) và 5 ml ethyl acetat (TT), khuấy rồi để yên 10 min trong nước đá. Lọc hút chân không qua phễu lọc thủy tinh xốp (cỡ 40). Lấy phần tinh thể, rửa với 5 ml nước và 5 ml ethyl acetat (TT), sấy ở 60 °C trong 60 min. Phổ hấp thụ hồng ngoại (Phụ lục 4.2) của tinh thể thu được phải phù hợp với phổ hấp thụ hồng ngoại của piperacilin chuẩn.
B. Chế phẩm phải cho phản ứng (A) của natri (Phụ lục 8.1).
Xem thêm: VIÊN NÉN PHYTOMENADION (Tabellae Phytomenadioni) – Dược Điển Việt Nam 5
Độ trong và màu sắc của dung dịch
Dung dịch S: Hòa tan 2,50 g chế phẩm trong nước không có carbon dioxyd (TT) và pha loãng thành 25 ml với cùng dung môi.
Dung dịch S phải trong (Phụ lục 9.2) và có độ hấp thụ ánh sáng ở bước sóng 430 nm không được quá 0,10 (Phụ lục 4.1).
pH
Dung dịch S phải có pH từ 5,0 đến 7,0 (Phụ lục 6.2).
Góc quay cực riêng
Từ+175° đến +190°, tính theo chế phẩm khan (Phụ lục 6.4).
Hòa tan 0,250 g chế phẩm trong nước và pha loãng thành 25,0 ml với cùng dung môi.
Tạp chất liên quan
Phương pháp sắc ký lỏng (Phụ lục 5.3).
Pha động A: Trộn đều 576 ml nước, 200 ml dung dịch natri dihydrophosphat (TT) 3,12 % và 24 ml dung dịch tetrabutylamoni hydroxyd (TT) 8 %, điều chỉnh đến pH 5, 5 nếu cần bằng dung dịch acid phosphoric loãng (TT) hoặc dung dịch natri hydroxyd loãng (TT), thêm 200 ml acetonitril (TT), lắc đều.
Pha động B: Trộn đều 126 ml nước, 200 ml dung dịch natri dihydrophosphat 3,12 % và 24 ml dung dich tetrabutylamoni hydroxyd 8 %, điều chỉnh đến pH 5,5 nếu cần bằng dung dịch acid phosphoric loãng (TT) hoặc dung dịch natri hydroxyd loãng (TT), thêm 650 ml acetonitril (TT), lắc đều.
Hỗn hợp dung môi: Acetonitril – dung dịch natri dihydrophosphat 3,12 % (25 : 75).
Dung dịch thử: Chuẩn bị ngay trước khi dùng, hòa tan 40.0 mg chế phẩm trong hỗn hợp dung môi và pha loãng thành 20,0 ml với cùng hỗn hợp dung môi.
Dung dịch đối chiếu (1): Hòa tan 25,0 mg piperacilin chuẩn trong hỗn hợp dung môi và pha loãng thành 50,0 ml với cùng hỗn hợp dung môi.
Dung dịch đối chiếu (2): Pha loãng 1,0 ml dung dịch đối chiếu (1) thành 25,0 ml bằng hỗn hợp dung môi.
Dung dịch đối chiếu (3): Pha loãng 1,0 ml dung dịch đối chiếu (1) thành 100,0 ml bằng hỗn hợp dung môi. Hút 1.0 ml dung dịch thu được pha loãng thành 50,0 ml với cùng hỗn hợp dung môi.
Dung dịch phân giải: Hòa tan 10,0 mg piperacilin chuẩn và 10,0 mg ampicilin khan chuẩn (tạp chất A) trong hỗn hợp dung môi và pha loãng thành 50,0 ml với cùng hỗn hợp dung môi.
Điều kiện sắc ký:
Cột thép không gỉ (25 cm x 4,6 mm) được nhồi pha tĩnh C (5 μm).
Detector quang phổ tử ngoại đặt ở bước sóng 220 nm.
Tốc độ dòng: 1,0 ml/min.
Thể tích tiêm: 20 μl.
Cách tiến hành:
Tiến hành sắc ký theo chương trình dung môi như sau:
| Thời gian | Pha động A | Pha động B |
| (min) | (%) | (%) |
| 0 – tR | 88 | 12 |
| tR – (tR +30) | 88 → 0 | 12 → 100 |
| (tR +30) – (tR +45) | 0 → 88 | 100 → 12 |
tR là thời gian lưu của pic piperacilin trên sắc ký đồ thu được từ dung dịch đối chiếu (2).
Nếu cần phải điều chỉnh thành phần pha động để đạt được độ phân giải theo yêu cầu thì phải áp dụng việc điều chỉnh ở thời điểm 0 của chương trình dung môi.
Tiến hành sắc ký các dung dịch đổi chiếu (2), (3) và dung dịch phân giải với pha động đẳng dòng theo tỷ lệ ban đầu của chương trình dung môi. Tiến hành sắc ký dung dịch thử với chương trình pha động ghi trong bảng.
Kiểm tra tính phù hợp của hệ thống: Trên sắc ký đồ của dung dịch phân giải, độ phân giải giữa pic tạp chất A và pic piperacilin không được nhỏ hơn 10, điều chỉnh tỷ lệ pha động A : Pha động B nếu cần. Hệ số phân bố khối lượng tính theo pic piperacilin phải từ 2,0 đến 3,0.
Trên sắc ký đồ của dung dịch đối chiếu (3): Tỷ số tín hiệu trên nhiễu của pic chính không được nhỏ hơn 3.
Giới hạn: Trên sắc ký đồ của dung dịch thử, không có pic tạp chất nào có diện tích lớn hơn 2 lần diện tích pic chính thu được trên sắc ký đồ của dung dịch đối chiếu (2) (2 %).
N,N-Dimethylanilin
Không được quá 20 phần triệu (Phụ lục 10.16, phương pháp 1).
Kim loại nặng
Không được quá 20 phần triệu (Phụ lục 9.4.8).
Lấy 1,0 g chế phẩm để thử theo phương pháp 3. Dùng 2 ml dung dịch chì mẫu 10 phần triệu Pb (TT) để chuẩn bị mẫu đối chiếu.
Nước
Không được quá 2,0 % (Phụ lục 10.3).
Dùng 0,500 g chế phẩm.
Xem thêm: PILOCARPIN NITRAT (Pilocarpini nitras) – Dược Điển Việt Nam 5
Nội độc tố vi khuẩn
Không được quá 0,07 IU/mg (Phụ lục 13.2).
Nếu chế phẩm được dùng để sản xuất các dạng thuốc tiêm mà không có phương pháp hữu hiệu loại bỏ nội độc tố vi khuẩn thì phải đáp ứng yêu cầu của phép thử này.
Định lượng
Phương pháp sắc ký lỏng (Phụ lục 5.3).
Pha động A, pha động B, hỗn hợp dung môi, điều kiện sắc ký như mô tả ở mục Tạp chất liên quan.
Pha động: Pha động A – pha động B (88 : 12), điều chỉnh tỷ lệ nếu cần.
Dung dịch thử: Hòa tan 25,0 mg chế phẩm trong hỗn hợp dung môi và pha loãng thành 50,0 ml với cùng hỗn hợp dung môi.
Dung dịch chuẩn: Dùng dung dịch đối chiếu (1) ở mục Tạp chất liên quan.
Cách tiến hành:
Kiểm tra tính phù hợp của hệ thống: Độ lệch chuẩn tương đối của diện tích pic trên sắc ký đồ của 6 lần tiêm lặp lại dung dịch chuẩn không lớn hơn 1,0 %.
Tiến hành sắc ký các dung dịch thử và dung dịch chuẩn.
Tính hàm lượng piperacilin natri, C23H26N5Na07S, trong chế phẩm dựa vào diện tích pic trên sắc ký đồ của dung dịch thử, dung dịch chuẩn và hàm lượng của piperacilin chuẩn, với hệ số hiệu chỉnh từ piperacilin sang piperacilin natri là 1,042.
Bảo quản
Trong đồ đựng kín. Nếu chế phẩm vô khuẩn thì bảo quản trong đồ đựng kín, vô khuẩn.
Loại thuốc
Thuốc kháng sinh nhóm penicilin.
Chế phẩm
Bột pha tiêm.